10-11月细胞行业动态 | 国家立法引领+核心技术赋能,激活产业创新动能
2025年第四季度,中国细胞与基因治疗(CGT)领域的发展画卷格外夺目。政策、技术与应用三股力量交织并进,共同奏响了一曲从规范确立到临床突破,再到惠及民生的产业交响乐。一个更规范、更创新、更可及的行业发展新阶段,正加速向我们走来。
01 政策引领
国家与地方协同,筑牢产业发展根基
2025年10-11月,生物医药产业政策密集落地,国家层面以专项立法划定行业发展的合规边界,地方则结合区域特色出台产业扶持与监管创新举措,从顶层设计到地方实践,构建起全方位、多层次的政策支撑体系,为细胞与基因治疗产业高质量发展保驾护航。
● 10月10日:《生物医学新技术临床研究和临床转化应用管理条例》公布,这是我国首次针对生物医学新技术临床研究与转化应用出台专项行政法规,标志着细胞与基因治疗领域迈入法治化、规范化管理新阶段。
● 10月21日:广州市公布细胞与基因产业布局及支持政策,计划2030年建成全链条产业生态,形成超千亿级产业集群,打造全球细胞与基因治疗创新策源地和产业发展高地。
● 11月1日:《重庆市全链条支持创新药高质量发展若干措施》发布,提出25条举措,明确2027年创新药发展目标,从多维度助力重庆打造生物医药产业高地。

● 11月24日:天津发布基因与细胞治疗新规,通过分类分级管理破解监管难题,缩短审批周期,为全国提供可复制的产业发展经验。
02 技术开花
临床与新药审批双线并进,创新疗法持续涌现
在明确的政策指引下,产业创新的“核心引擎”全力驱动。10-11月,CGT领域在临床试验与新药研发上呈现持续的活力与广度。
10月份,共计19款CGT药物的临床试验申请获国家药品监督管理局药品审评中心(CDE)审批。产品类型覆盖iPSC药物、间充质干细胞药物、T细胞药物及基因治疗药物等多类创新疗法,涉及缺血性脑卒中偏瘫后遗症、早发型帕金森病、原发性膝骨关节炎、胶质母细胞瘤、多系统萎缩症等十余种适应症。既展现出国内CGT技术在不同治疗领域的多元布局,也标志着该领域在临床转化阶段的加速推进。
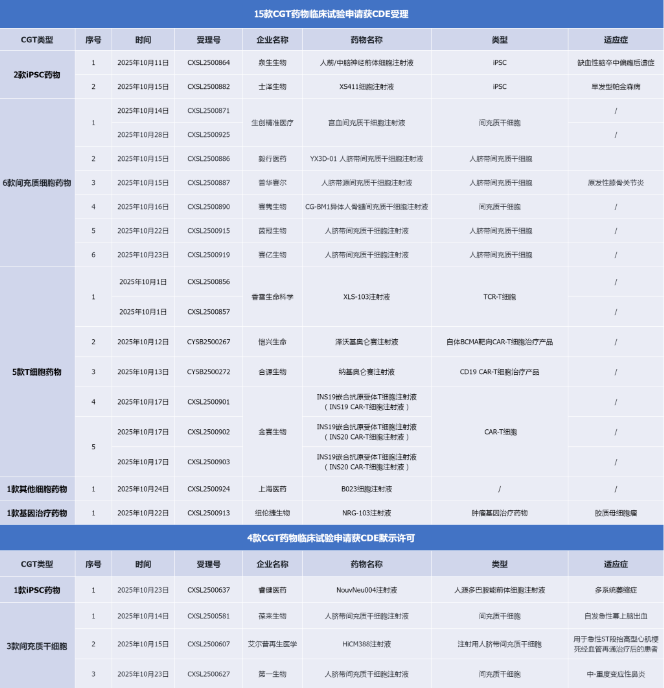
▲2025年10月国内获批临床试验的CGT疗法、核酸药物
进入11月,共有12款细胞与基因治疗(CGT)及核酸类药物获批临床,产品类型覆盖自体TRT、异体NK、脐带MSC以及即用型iNKT,并从传统肿瘤治疗逐步拓展至免疫与炎症性疾病。
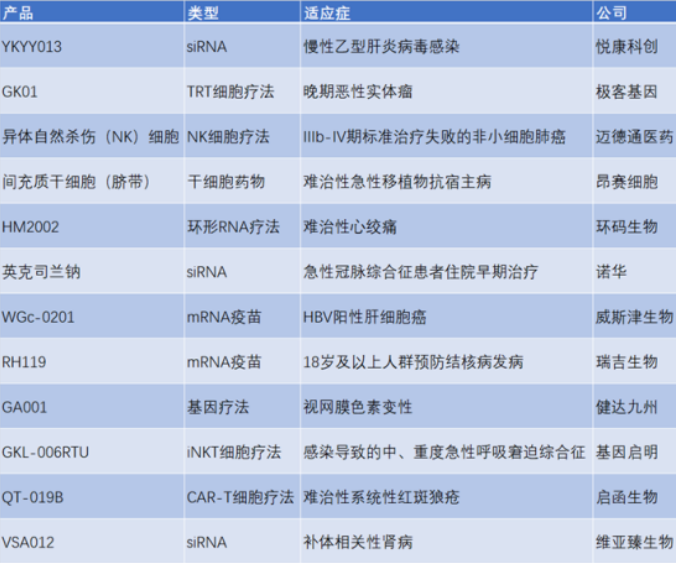
▲2025年11月国内获批临床试验的CGT疗法、核酸药物
并有4款细胞类Ⅰ类新药的临床申请顺利进入受理阶段。包括1款自体NK细胞注射液、1款多能干细胞衍生胰岛细胞注射液,以及2款分别源自脐带和宫血的间充质干细胞(MSC)制剂。适应症覆盖恶性实体瘤、1型糖尿病、炎症性肠病、肺纤维化等领域。
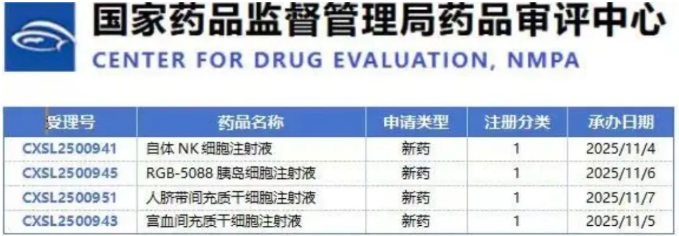
▲临床申请已进入受理阶段的4款细胞类Ⅰ类新药
03 普惠落地
价格透明与医保覆盖并行,提升“可及性”
价格透明:
博鳌新增6项干细胞治疗技术,最低5万元/次
11月,乐城新增获批6项干细胞治疗技术,截至目前,博鳌乐城已累计四批共15项干细胞临床技术通过特许使用审批,这些项目覆盖范围极广:从肿瘤免疫到心血管疾病,从糖尿病到黄斑变性,再到类风湿关节炎与牙周病修复,几乎囊括了当前干细胞研究的主流方向。15项名单的发布,不只是科学突破,更是监管体系的一次信号释放——中国的干细胞疗法,开始走上合法、规范、临床转化的正轨。
医保推进:
首款干细胞药物正式纳入北京惠民保
11月,“北京普惠健康保”将我国已获批的干细胞药物——艾米迈托赛注射液(睿铂生) 纳入特药目录,参保患者符合条件费用最高可报销65%。这不仅是该药品在商业保险支付上的重大突破,更标志着CGT疗法正在被更广泛的社会保障体系所接纳,切实减轻了重症患者的经济负担。(该药用于治疗激素治疗失败的急性移植物抗宿主病(aGVHD),已于今年6月在北京大学人民医院实现首张处方落地。)
政策绘制了产业发展的“航道图”,技术突破则成为推动行业前进的“发动机”。在政策保障、技术攻坚与市场需求的三重驱动下,中国细胞与基因治疗产业正稳步走向规范化、创新化、普惠化的发展新阶段,前沿科技正逐步转化为守护人民健康的坚实力量。


 扫一扫,关注我们
扫一扫,关注我们
