解析CDMO中试基地与基础实验室的核心差异(下篇)
理清CDMO中试基地与基础实验室的差异后,更能明确专业CDMO中试基地的独特价值。山东丽山生物科技有限公司凭借免疫细胞与基因治疗(CGT)领域的全链条能力,成为合作伙伴实现成果转化的优选。

▲山东省免疫细胞与基因治疗CDMO中试基地实景
价值逻辑:
产业转化与知识创新的双重追求
CDMO中试基地与基础实验室的差异,最终体现在价值产出的导向不同,这种导向决定了二者的商业逻辑与社会功能。
1
基础实验室:
知识创新与技术突破
基础实验室的价值核心是知识创新与技术突破,成果多以论文、专利呈现,虽能为产业提供理论基础与早期技术储备,但自身无法完成中试转化与临床落地。

▲部分专利展示
2
CDMO中试基地:
产业转化与商业实现
CDMO中试基地的价值核心是产业转化与商业实现,通过中试环节将基础实验室成果转化为可产业化的产品,推动医药产品上市进程。
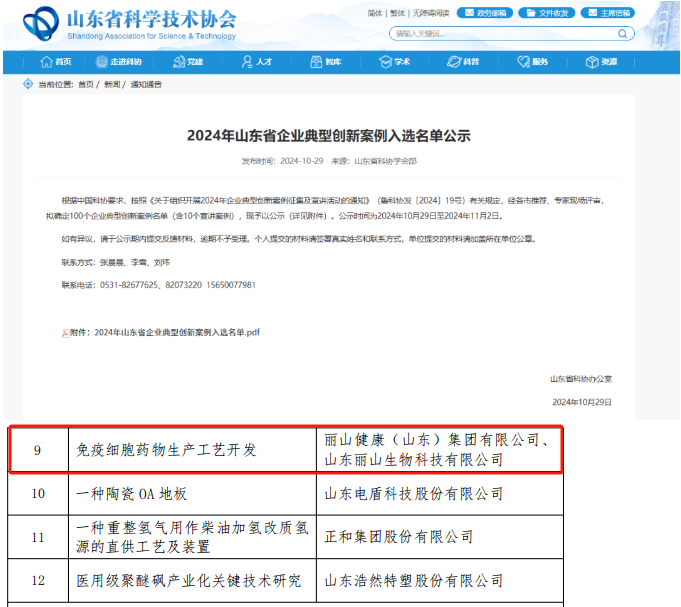
丽山生物的价值逻辑尤为清晰:其“通用型CAR-NK细胞药物产业化平台”项目获2025生物制造创新创业大赛优胜奖,研发的质粒制备中试工艺入选山东省企业典型创新案例,这些成果直接服务于客户的产业化目标,帮助合作伙伴加速中试转化进程、降低商业化成本,这正是产业端最迫切的需求。
▲2025生物制造创新创业大赛优胜奖
丽山生物:
CGT产业化合作的核心优势
对于创新药企、高校及科研机构而言,选择丽山生物,本质上是选择了一条高效、合规、低成本的“基础实验室成果-中试转化-产业落地”路径。其核心优势可概括为三点:
1
权威认证的中试平台保障
丽山生物是山东省首家省级认可的CGT CDMO中试基地,具备合规化、规模化中试服务的先天优势。平台资质经过严格审核,符合监管要求,能为合作伙伴提供稳定、可靠的中试环境,规避资质不合规带来的风险。

▲示意图
2
全链条的中试技术能力
丽山生物通过三大核心平台——免疫细胞与基因治疗CDMO中试基地、基因测序与合成中心、济南(丽山)区域细胞组织库及细胞制备中心,协同构建了覆盖“研发-中试-生产”等的全链条服务体系。

▲三大核心平台实景
合作伙伴无需对接多个合作方,即可完成从非注册临床研究、IND申报、临床试验到商业化生产的全阶段需求,服务产品涵盖质粒、LV/AAV载体、CAR-T、CAR-NK等多个品类,大幅提升转化效率。
3
降本增效的中试实战成果
丽山生物在中试工艺优化上积累了丰富的实战经验,能切实解决基础实验室成果 “转化难、成本高、周期长” 的行业痛点。例如,其研发团队通过基因改造生产菌株,使质粒产量翻倍、成本降至原来的一半;将NK细胞编辑率提升至97%,远超行业普遍水平;开发的CAR-T制备工艺经中试验证,细胞活性稳定在95%以上,相关技术达“国际先进水平”。这种融合了研发、中试工程、成本控制的综合能力,正是基础实验室的短板所在,也是丽山生物CDMO中试基地的核心优势。同时,其建立的快速响应机制,能及时应对中试过程中的问题,缩短转化周期。

▲实验室实景
结语:
MAH 制度下的产业协同逻辑
在MAH(药品上市许可持有人)制度日益完善的背景下,基础实验室与CDMO中试基地形成了“创新种子+最优培育生态”的协同模式。基础实验室提供“创新种子”,丽山生物CDMO中试基地则打造“最优培育生态”,通过专业化服务推动创新成果快速落地。
选择丽山生物,就是选择让基础实验室创新成果快速落地、实现商业价值的专业伙伴,这正是其成为CGT产业化合作不二之选的核心逻辑。


 扫一扫,关注我们
扫一扫,关注我们
